随着非小细胞肺癌(NSCLC)治疗理念的不断精进,以免疫治疗为基础的方案正持续重塑着患者的治疗路径。以纳武利尤单抗为例,其方案在2026版《CSCO非小细胞肺癌诊疗指南》(以下简称《指南》)的更新中再次迎来两项重要的推荐更新,有望进一步优化国内NSCLC的诊疗策略:
· 在晚期治疗领域,基于CheckMate-227研究成果及临床可及性的提升,纳武利尤单抗联合伊匹木单抗(“O+Y”)方案被升级为Ⅳ期无驱动基因NSCLC治疗的Ⅱ级推荐,进一步巩固了“免化疗”双免方案在晚期肺癌中的治疗地位。
· 与此同时,基于CheckMate-77T研究成果及临床可及性的提升,纳武利尤单抗联合化疗用于可切除NSCLC围术期治疗的推荐等级也升级至Ⅰ级。
为此,《中国医学论坛报》特邀《指南》执笔专家、中国医学科学院肿瘤医院(884301)段建春教授,结合指南更新亮点,深度解读“O+Y”双免疗法的疗效突破以及纳武利尤单抗在NSCLC中的临床价值,以期为临床实践提供更多参考。
晚期NSCLC:一线O+Y双免方案升级为Ⅱ级推荐,CheckMate-227六年生存数据筑牢循证基石
目前,PD-(L)1抑制剂±化疗已成为驱动基因阴性晚期NSCLC患者的一线标准方案。然而,PD-L1低表达、携带特殊突变、化疗不耐受等特殊人群的治疗仍面临一定挑战,临床策略亟待进一步优化。
在此背景下,《指南》的一项更新尤为引人注目:在Ⅳ期无驱动基因非鳞NSCLC的一线治疗领域,纳武利尤单抗+伊匹木单抗(O+Y)方案被升级为Ⅱ级推荐(限PD-L1 TPS≥1%患者)。此前,国家药品监督管理局(NMPA)已正式批准O+Y方案用于PD-L1 TPS≥1%的晚期NSCLC一线治疗,使其成为中国首个肺癌一线双免疗法,填补了国内该领域的长期空白。此次《指南》推荐等级的升级,进一步确立了O+Y方案在晚期肺癌一线治疗中的重要地位,也标志着晚期NSCLC的一线治疗格局正稳步迈向“免化疗”的新时代。
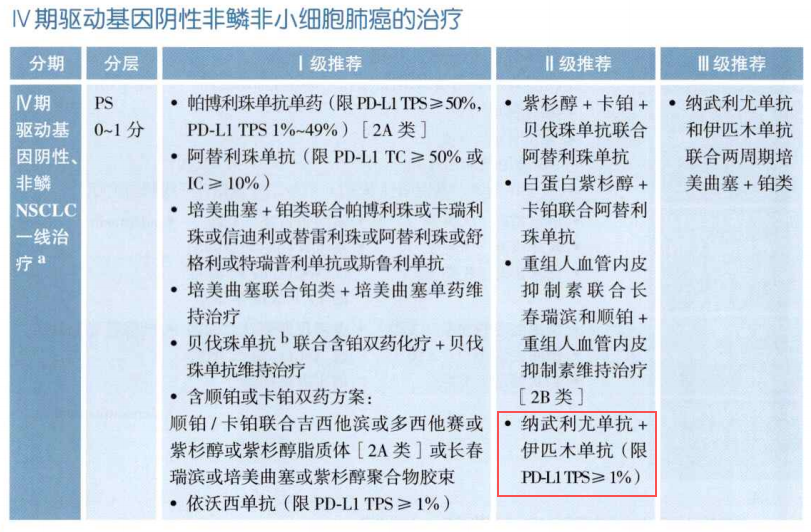
图1. 2026 CSCO指南在Ⅳ期驱动基因阴性非鳞NSCLC的一线治疗策略推荐
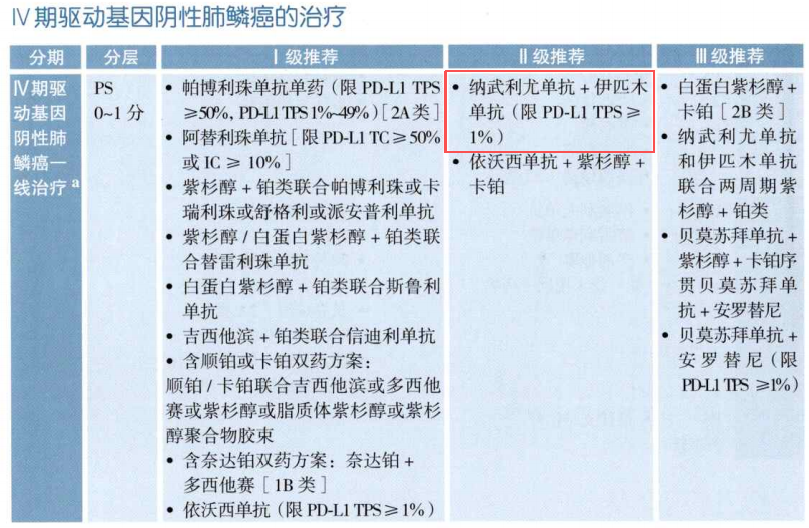
图2. 2026 CSCO指南在Ⅳ期驱动基因阴性肺鳞癌的一线治疗策略推荐
全球III期研究CheckMate-227的6年生存数据为一线O+Y方案推荐等级的提升提供了坚实的循证支撑[1]。在主要终点人群(PD-L1 TPS≥1%)中,O+Y组中位总生存(OS)延长至17.1个月(化疗组14.9个月,HR=0.78),6年OS率达22%,而化疗组仅为13%,展现出稳定而持续的生存获益。尤为值得关注的是,O+Y方案的生存曲线后期呈现出明显的“平台期”效应:从第5年至第6年,OS率下降幅度仅2%。这一持久的“长拖尾”效应,深刻诠释了免疫治疗一旦起效、长期获益的独特优势。

图3. CheckMate-277研究PD-L1≥1%患者6年生存数据
在追求延长生存的同时,CheckMate-227研究还重点关注了患者的治疗负担与生活质量。CheckMate-227研究发表于《Journal of Thoracic Oncology》的无治疗生存期(TFS)分析结果显示[2],O+Y组患者TFS长达12.2个月,是化疗组(仅5.0个月)的2倍以上。这意味着接受O+Y方案的患者,在其生存期内有更多的时间处于无需任何抗肿瘤治疗的状态。此外,在接受O+Y治疗后达到5年生存的患者中,高达66%在停药后超过3年未再接受任何后续全身治疗。由此可见,O+Y方案不仅致力于延长生命的长度,也践行了“高质量长期生存”的现代肿瘤治疗理念。
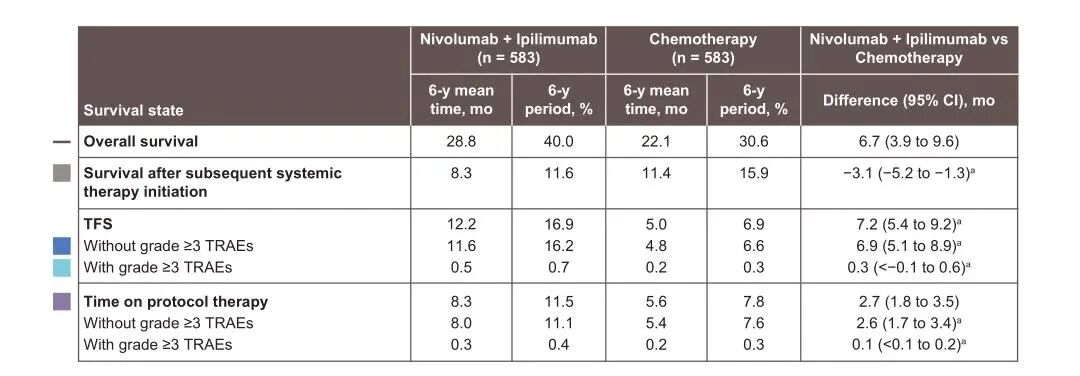
图4. CheckMate-277研究总人群TFS数据
在真实世界临床实践中,O+Y方案还具备多重现实优势。对于因年龄、体力状态(PS评分)或合并症而不耐受或拒绝含铂双药化疗的患者,O+Y提供了一种高效且免化疗的新选择。此外,伊匹木单抗采用1mg/kg,Q6W的低剂量、长间隔给药方案,在确保抗肿瘤疗效的同时,免疫相关不良事件的发生风险也较低。随着该方案在中国临床的广泛落地,晚期NSCLC的一线治疗正迎来“双免时代”,有望为广大晚期肺癌患者带来兼顾生存长度与生活质量的双重获益。
突破免疫“禁区”:O+Y为KEAP1/STK11突变及PD-L1阴性人群提供新选择
在晚期NSCLC的免疫治疗中,并非所有患者都能同等获益。KEAP1/STK11突变被公认为免疫治疗的负向预测因子,在NSCLC中的发生率约为10~20%[3]。此类患者的肿瘤微环境呈现典型的“冷肿瘤”特征,对PD-1/PD-L1±化疗的应答十分有限,临床预后不佳,未满足需求较为突出[4]。而CheckMate-227研究的探索性分析数据显示[5],O+Y双免方案在KEAP1/STK11突变患者中展现出获益趋势,带来了全新的破局思路。
数据显示,在携带KEAP1突变的患者中,O+Y方案的4年OS率高达44%,而同期化疗组则为0%;HR低至0.31,死亡风险降低69%。
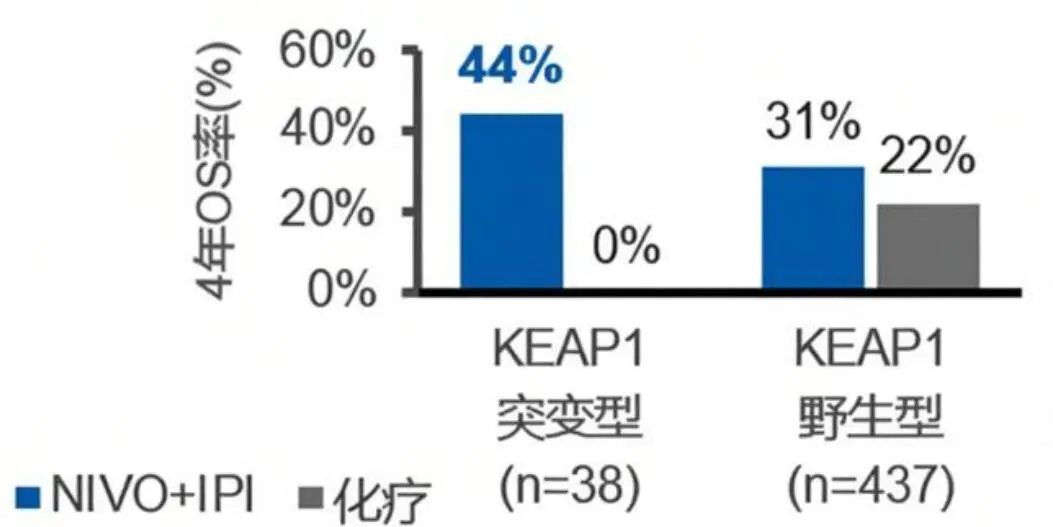
图5. CheckMate-277研究探索性分析KEAP1突变患者4年OS率
无独有偶,在STK11突变人群中亦观察到良好的生存获益信号:O+Y组4年OS率达19%,明显优于化疗组的5%(HR=0.78)。这一系列令人鼓舞的生存数据提示,CTLA-4抑制剂的加入可能在打破免疫耐受、重塑抗肿瘤免疫反应方面发挥关键作用,使O+Y双免方案成功突破了既往分子亚型的治疗限制。
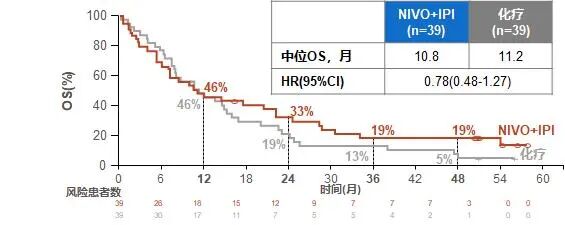
图6. CheckMate-277研究探索性分析STK11突变患者4年OS率
上述临床观察在机制研究中得到了进一步验证。研究显示[6],在KEAP1、STK11突变的肿瘤微环境中,CTLA-4抑制剂的加入发挥着关键的“免疫重塑”作用,可显著增加 CD4+ 效应 T 细胞(尤其是 Th1)的应答,并促进髓系细胞向 iNOS(诱导型一氧化氮合酶,即肿瘤杀伤型细胞)高表达的促炎表型转化,从而重塑这类患者的免疫微环境,为PD-1抑制剂起效扫清障碍。
值得关注的是,即使在传统意义上对免疫治疗响应较差的PD-L1阴性(TPS<1%)人群中,O+Y方案同样展现出持续而稳定的长期生存获益潜力。数据显示[1],O+Y组6年OS率达16%,相较于化疗组的5%明显提升,死亡风险降低35%(HR=0.65)。
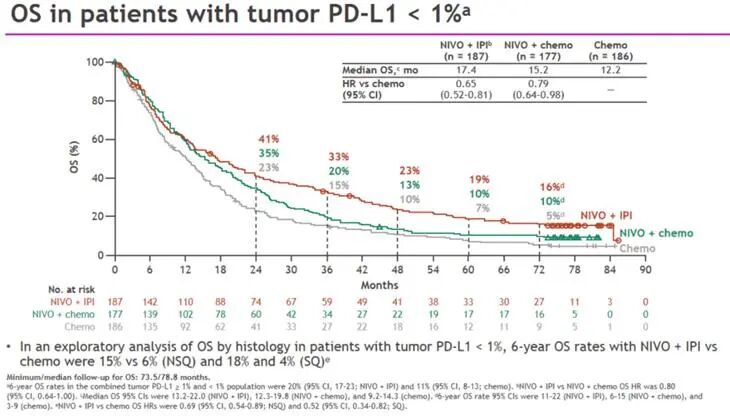
图7. CheckMate-277研究PD-L<1%患者6年生存数据
这一结果进一步提示,O+Y双免方案发挥抗肿瘤免疫效应可能并不完全依赖于PD-L1表达水平,而是通过独特的免疫激活机制,实现了对“冷肿瘤”人群的广泛覆盖。例如,伊匹木单抗还可通过其独特的抗体依赖的细胞介导细胞毒性(ADCC)效应,高效清除肿瘤微环境中的调节性T细胞(Treg),从而解除局部免疫抑制状态,为效应T细胞的激活与扩增扫清障碍。这一过程将原本“免疫冷”的肿瘤微环境,成功转化为对免疫治疗更为敏感的“热肿瘤”,使纳武利尤单抗得以更充分地发挥其抗肿瘤免疫效应,两者协同作用,并最终实现在传统免疫“禁区”人群中的疗效突破。
早期NSCLC:纳武利尤单抗围术期治疗进阶为Ⅰ级推荐,引领治疗新格局
继CheckMate-816研究推动纳武利尤单抗获批可切除NSCLC新辅助治疗后,2025年4月,基于CheckMate-77T研究,NMPA批准纳武利尤单抗用于可切除NSCLC的围术期(新辅助+辅助)治疗。此次,《指南》针对可切除NSCLC的治疗推荐进行了同步更新,将“含铂化疗联合纳武利尤单抗新辅助+辅助治疗”方案升级为Ⅰ级推荐。由此,纳武利尤单抗成为目前唯一同时获得NSCLC新辅助与围术期方案Ⅰ级推荐的免疫治疗药物。从指南循证学角度来看,这一推荐也为以纳武利尤单抗为基础的围术期应用提供了有力佐证,更充分验证了其在新辅助治疗与辅助治疗场景中灵活应用的科学性与临床可行性。

图8. 2026 CSCO指南在ⅡA、ⅡB期NSCLC治疗的策略推荐

图9. 2026 CSCO指南在可手术ⅢA或ⅢB(T3N2M0)期NSCLC治疗的策略推荐
CheckMate-77T研究的数据为这一指南升级奠定了坚实的循证基础[7]。中位随访33.3个月时,纳武利尤单抗组的主要终点中位无事件生存期(EFS)达40.1个月,较对照组(17.0个月)延长近两年,疾病进展、复发或死亡风险降低41%(HR=0.59)。
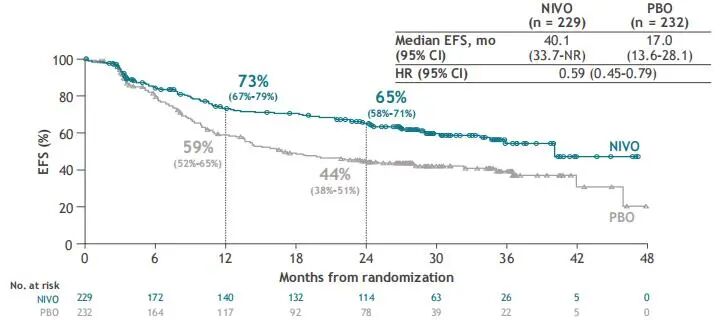
图10. CheckMate-77T研究全球人群的EFS数据
在病理学缓解方面,纳武利尤单抗组同样展现出明显优势[8]:病理学完全缓解(pCR)率达25.3%,明显优于对照组的4.7%;主要病理缓解(MPR)率达35.4%,亦优于对照组的12.1%。这一更深层次的病理缓解不仅有助于提高手术根治性,更与患者的远期预后密切相关,并有望进一步转化为长期生存优势。安全性方面,纳武利尤单抗组未发现新的安全性信号,不良事件谱与既往已知特征一致,总体可控、可管理。
进一步分析显示,CheckMate-77T研究在不同亚组患者中均呈现出较为一致的疗效趋势,尤其在中国患者亚组中[9],纳武利尤单抗组的中位EFS尚未达到,而对照组为12.6个月,疾病复发、进展或死亡风险降低60%(HR=0.40);同时,pCR率(35.1% vs. 3.2%)与MPR率(51.4% vs. 6.5%)均明显优于对照组。上述结果提示,纳武利尤单抗围术期方案在中国患者人群中呈现的获益与全球人群一致,且疗效数据上更为亮眼。
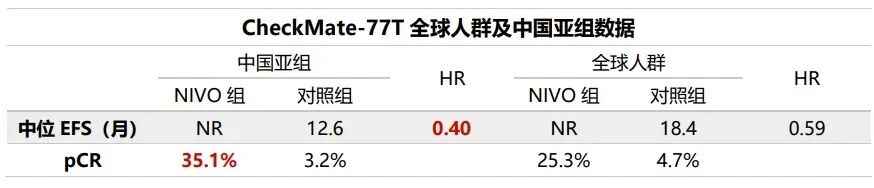
图11. CheckMate-77T中国亚组与全球人群疗效数据
总结
在晚期NSCLC一线治疗领域,O+Y双免方案基于CheckMate-227研究长达6年的生存优势,并展现出跨越PD-L1表达水平限制、覆盖KEAP1/STK11等特殊突变人群的独特价值,升级为《指南》Ⅱ级推荐,进一步推动了“免化疗”双免疗法在我国临床实践中的推广与应用。
在围术期治疗领域,纳武利尤单抗作为唯一同时获得NSCLC新辅助与围术期方案Ⅰ级推荐的免疫治疗药物,进一步丰富了临床选择,同时促进了早期NSCLC围术期全程管理的优化升级。
展望未来,随着高质量循证医学证据的不断积累与临床实践的持续深化,纳武利尤单抗有望逐步构建起覆盖早期乃至晚期NSCLC的全程治疗布局,使免疫治疗的优势贯穿于肺癌治疗的全周期(883436),并助力更多肺癌患者实现更长生存、更优生活的美好愿景。
专家简历

